
En ny analyse viser, at over to tredjedele af ansøgningerne til Medicinrådet er forsinket med mere end to måneder. ”Medicinrådet har fået flere penge til at håndtere flere ansøgninger, og det er tiltrængt, for vi ser desværre ikke nogen forbedringer på kort sigt,” siger Louise Broe, politisk chef for sygehusmedicin i Lif.
Medicinrådet har fokus på at overholde sagsbehandlingstiderne og meldte i marts ud, at man ville blive presset på kapaciteten og formentlig så ind i overskridelser af sagsbehandlingstiderne på grund af flere ansøgninger end forventet på trods af en række indsatser.
I juli i år kunne nye tal fra Lægemiddelindustriforeningen, Lif, så bekræfte den forudsigelse, og at der ofte går lang tid med at komme i gang med vurderingerne i Medicinrådet.
Og nu ser situationen desværre ud til at være blevet en smule forværret, viser en ny analyse fra Lif.
Flere virksomheder får besked på at vente med at sende deres ansøgning, og de venter i længere tid.
Hvor der i juli 2025 var 41 virksomheder, der fik udskudt deres ansøgning med 68 dage i gennemsnit, så er det tal nu 54 virksomheder, som i gennemsnit får udskudt ansøgningen med 71 dage – over to måneder.
”Vi er selvfølgelig meget optaget af, at nye innovative lægemidler hurtigt kan tages i brug i behandlingen af danske patienter. Det ved vi også optager Medicinrådet, og derfor er det en frustrerende udvikling, som vi ser frem til, at der bliver rettet op på med flere ressourcer og mindre bureaukratiske processer,” siger Louise Broe, politisk chef for sygehusmedicin i Lif.
Hun peger på, at lange ventetider på at ansøge Medicinrådet ikke bare har konsekvenser for virksomhederne.
”Vi følger løbende udviklingen, fordi forsinkelser i sidste ende betyder, at patienter må vente længere på at få adgang til nye behandlinger,” siger hun.
Virksomhederne har siden april 2024 skulle angive et ønsket ansøgningstidspunkt, når de sender en anmodning om vurdering af et lægemiddel til Medicinrådet. Oftest bliver en udskydelse begrundet med manglende kapacitet i det pågældende fagudvalg.
Vi mener, at nogle processer er unødigt bureaukratiske og retningslinjerne nok lidt for ufleksible. Medicinrådet har allerede effektiviseret meget, men mere kan gøres.
Der er brug for at tænke nyt
Udskydelse af ansøgningstidspunktet kommer oveni, at også de maksimale sagsbehandlingstider overskrides.
Faktisk tager det nu i gennemsnit en måned længere end de 18 uger, der er den politisk fastsatte målsætning for tiden til vurderinger af nye innovative lægemidler.
I oktober blev det derfor for andet år i træk meldt ud, at Danske Regioner tilførte Medicinrådet ekstra millioner for at imødekomme udfordringerne.
”Det er positivt, at Medicinrådet har fået flere ressourcer, men udviklingen viser også, at der er behov for andet end flere penge. Vi mener, at nogle processer er unødigt bureaukratiske og retningslinjerne nok lidt for ufleksible. Medicinrådet har allerede effektiviseret meget, men mere kan gøres,” siger Louise Broe.
En af det ting, man ifølge Lif kan gøre, er at forenkle Medicinrådets fast-track-proces, så den bliver hurtigere og mere enkel, ligesom der bør tænkes i en fast-track-proces for flere typer lægemidler, fx indikationsudvidelser.
”Fast track skal være netop det – en hurtig og mere simpel vej. Derfor bør velkendte behandlinger, hvor vi kender effekt og økonomi godt, ikke igennem samme omfattende vurdering. Her kan spares tid og kapacitet for Medicinrådet og virksomhederne,” siger Louise Broe.
Lif mener også, at Medicinrådet kan spare nogle ressourcer ved at kriterierne for revurdering af lægemidler, som ikke anbefales første gang, gøres mere tydelige.
“Det vigtigste for virksomhederne er selvfølgelig, at lægemidlet bliver anbefalet og taget i brug på de danske sygehuse. Men virksomhederne søger om revurdering lidt i blinde i dag. Derfor foreslår vi bedre vejledning til virksomheder om, hvad der skal til for at få en revurdering, så ingen spilder til på ansøgninger, hvis det er irrelevant,” siger Louise Broe og fortsætter:
”Og når det gælder lægemidler til små og sjældne sygdomme, må vi acceptere, at det er et vilkår, at evidensen ofte er sparsom grund af den lille patientgruppe. Det kan ikke løses i selve vurderingen af lægemidlet. Til gengæld skal vi blive bedre til at følge op med real-world data, når lægemidlerne bruges i praksis.”
Læs mere om tallene for juli 2025 her.
Dage mellem virksomhedens ønskede ansøgningstidspunkt og det aftalte ansøgningstidspunkt:
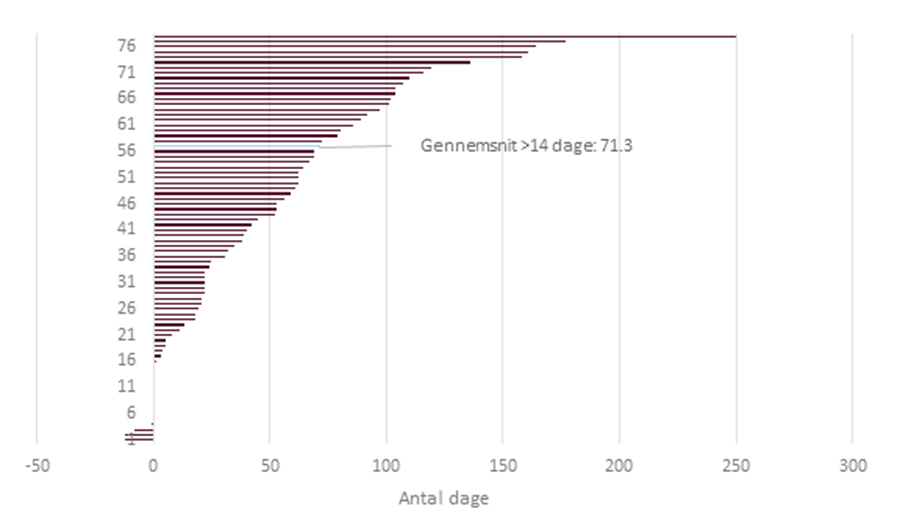
I analysen indgår data for 77 lægemidler, som Lifs medlemsvirksomheder har sendt til Medicinrådet med henblik på vurdering og modtaget et ansøgningstidspunkt for.
Fire af de 77 vurderinger har fået et ansøgningstidspunkt, som ligger tidligere end det ønskede – op til 12 dage før.
I 19 vurderinger har virksomheden fået det ønskede ansøgningstidspunkt eller en dato inden for 14 dage efter den ønskede dato.
I 54 tilfælde er ansøgningstidspunktet udskudt mere end 14 dage i forhold til det ønskede ansøgningstidspunkt.
De virksomheder, som har fået udskudt deres ansøgningstidspunkt mere end 14 dage i forhold til det ønskede, har i gennemsnit fået udskudt deres ansøgning i 71 dage – eller over to måneder.
Vi har kigget på at alle vurderinger siden det faste ansøgningstidspunkt blev indført i april 2024, og på de sager, hvor der fremgår et aftalt afsøgningstidspunkter. Vi har udvalgt vurderinger af lægemidler fra Lifs medlemsvirksomheder, og spurgt virksomhederne til det ønskede ansøgningstidspunkt. Det har vi sammenholdt med det aftalte ansøgningstidspunkt, som kan findes på Medicinrådets hjemmeside.
Lifs medlemmer har i alt haft 109 sager til vurdering siden april 2024, hvoraf nogle er afsluttet og nogle er fortsat under vurdering. Sager, som Medicinrådet har taget op af egen drift, indgår ikke i analysen. Vi har i den forbindelse data på ansøgningstidspunkter for 77 vurderinger. For en række af de vurderinger, hvor der ikke findes data, var der ikke fastsat et ansøgningstidspunkt af Medicinrådet per 1. oktober 2025, hvor Lif har spurgt virksomhederne til information.

