I alt er der stillet 32 spørgsmål, som indenrigs- og sundhedsminister Sophie Løhde nu har svaret på i forbindelse med behandlingen af lovforslaget om pligtlagre. Vi har udvalgt de seks mest interessante svar.
Spørgsmål 1: Hvem har udfordringer med forsyning?
”Vil ministeren redegøre for, hvor stor en andel af de lægemidler med eksempler på forsyningsudfordringer, som stammer fra henholdsvis parallelimportørerne og producenterne (generika og original)?”
Lægemiddelstyrelsen er ikke i besiddelse af en opgørelse, der viser, hvor stor en andel af forsyningsvanskeligheder for lægemidler, der stammer fra henholdsvis parallelimportørerne og producenterne. Det vil kræve længere tid at tilvejebringe en opgørelse, da det vil omfatte en større analyse af tilgængelige data, herunder fastlæggelse af metodiske forhold.
Spørgsmål 6: Antal sager med forsyningsvanskeligheder
”Vil ministeren bidrage med en liste over situationer fra de sidste ti år – eller en anden meningsfuld periode – hvor der har været en kritisk mangel på lægemidler, samt redegøre for, hvilke lægemidler, det har drejet sig om, og hvad årsagerne til mangelsituationen har været?”
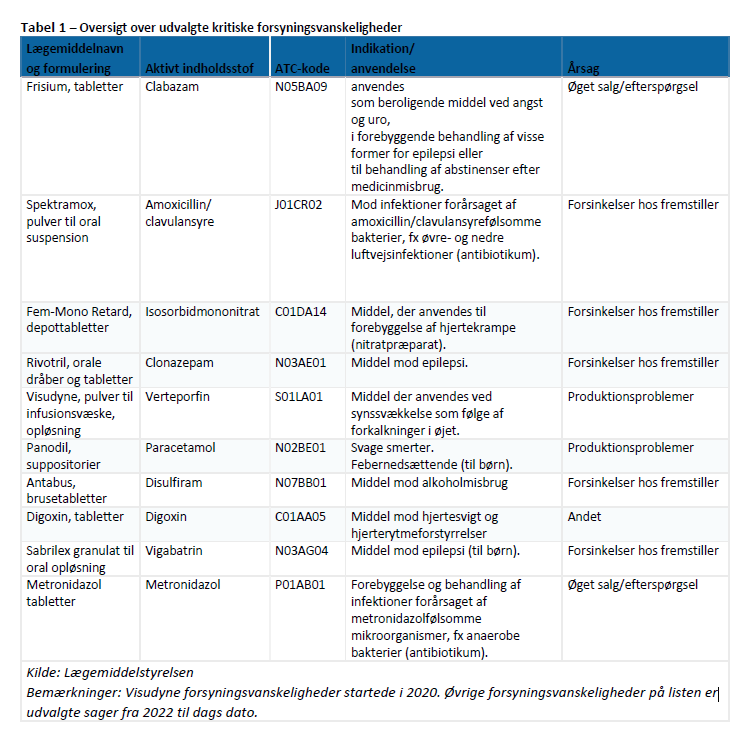
Lægemiddelstyrelsen kan opgøre sager om kritiske forsyningsvanskeligheder fra 31. marts 2020. Det er ikke muligt at gå længere tilbage. Lægemiddelstyrelsen har til besvarelse af spørgsmålet udarbejdet en tabel (tabel 1) over udvalgte kritiske forsyningsvanskeligheder for perioden 31. marts 2020 til dags dato. Tabel 1 fremgår nedenfor og indeholder lægemiddelnavn og form, aktive indholdsstof, ATC-kode, indikation/anvendelse af lægemidlet samt overordnet årsag til virksomhedens forsyningsvanskelighed. Det skal bemærkes, at ”kritisk” er defineret som situationer, hvor det ikke er muligt at finde et andet lægemiddel til behandling af patienten, og hvor en mangel kan have potentielt livstruende eller alvorlige sundhedsskadelige konsekvenser for patienten. Er lægemidlet tilgængeligt i en anden pakningsstørrelse eller findes der et markedsført, substituerbart lægemiddel, vil der ikke være tale om en kritisk forsyningsvanskelighed. Det samme gør sig gældende i situationer, hvor patienten kan skiftes over på et andet, ikke-substituerbart lægemiddel, for eksempel et lægemiddel på udleveringstilladelse eller et alternativt markedsført lægemiddel via ny recept fra lægen. Vurderingen af kritikalitet kan ændre sig undervejs i Lægemiddelstyrelsens sagsbehandling, for eksempel, hvis en anden virksomhed, som har samme/tilsvarende lægemiddel markedsført, kan levere mere end normalt af det i mangelperioden. Det indebærer, at en forsyningsvanskelighed, der indledningsvis er vurderet kritisk, ikke nødvendigvis ender med i en situation, der påvirker patientbehandlingen i kritisk grad. Håndtering af forsyningsproblemer koster megen tid og ressourcer hos myndighederne og i sundhedsvæsenet, men heldigvis resulterer håndteringen i, at vi sjældent oplever at en forsyningsvanskelighed betyder, at patienter står helt uden mulighed for medicinsk behandling. Det bemærkes, at grundlaget for, hvad der skal indberettes som forsyningsvanskeligheder til Lægemiddelstyrelsen siden juni 2023, har været Lægemiddelstyrelsens liste over kritiske lægemidler.
Spørgsmål 7: Erfaringer fra Holland og Frankrig
”I Holland og Frankrig har man allerede en ordning med lagerpligt. Vil ministeren redegøre for, hvilke lægemidler man tidligere har haft mangel på i de respektive lande, og hvordan den nye lagerpligt har bidraget til at sikre forsyningssikkerheden og gøre op med mangelsituationer?”
Indenrigs- og Sundhedsministeriet har ikke informationer om, hvilke lægemidler der tidligere har været mangel på i Nederlandene og Frankrig, eller om de konkrete effekter af landenes ordninger med lagerpligt for lægemiddelvirksomheder. Indenrigs- og Sundhedsministeriet har fået oplyst, at i Nederlandene har indehavere af markedsføringstilladelse og grossister siden 2007 været forpligtet til at sikre et tilstrækkeligt lager af apotekslægemidler, hvor indehavere af markedsføringstilladelse skal sikre et lager svarende til 6 ugers salg, og grossister skal sikre et lager svarende til 2 ugers salg. I Frankrig har indehavere af markedsføringstilladelse og virksomheder, der udbyder et lægemiddel på det franske marked, siden 2021 være forpligtet til at opbygge et sikkerhedslager til dækning af mindst 2 måneds behov for lægemidler af større terapeutisk betydning og minimum 1 uges behov for øvrige lægemidler.
Spørgsmål 12: Betaling af pligtlagre
”Mener ministeren, at det er rimeligt at lade borgere og patienter betale for opbygning af pligtlagre på lægemidler, sådan som det fremgår af bemærkningerne til lovforslaget – også selvom mange lægemidler på listen aldrig har været i restordre?”
Det er generelt vanskeligt at forudsige, hvilke lægemidler der bliver ramt af forsyningsproblemer. Derfor er det ikke tilstrækkeligt at se på, hvilke lægemidler der tidligere har været i restordre. Fastlæggelsen af, hvilke kritiske lægemidler, der skal være omfattet af lagerpligten, vil ske ud fra en vurdering af konsekvenser for patienterne ved mangel på et lægemiddel. Der vil blive lagt vægt på bl.a., om lægemidlerne er til behandling af tilstande og sygdomme, der kræver akut behandling eller er kroniske, og hvor manglende behandling på kort sigt kan medføre død, indlæggelse, varige mén eller væsentligt forringet livskvalitet, eller om skift til alternativ behandling medfører væsentlige patientsikkerhedsmæssige risici. Jeg er opmærksom på, at lovforslaget vil medføre omkostninger for virksomhederne, hvilket kan få konsekvenser for medicinpriserne. Derfor er det naturligvis væsentligt, at lagerpligten ikke bliver mere omfattende end nødvendigt. Jeg har lyttet til de input, der er kommet fra både offentlige og private aktører på området. Regeringen har på den baggrund tilpasset lovforslaget for at ramme den rette balance og mindske konsekvenserne for virksomhederne. For borgere vil mulige øgede medicinudgifter som følge af lovforslaget blive begrænset af gældende regler om medicintilskud til tilskudsberettiget medicin. Tilskudssystemet er indrettet sådan, at jo større udgifter patienten har til tilskudsberettiget medicin, jo mere får patienten i tilskud inden for en periode på ét år. Derudover er der et loft over, hvor meget den enkelte borger skal betale i løbet af den et-årige periode. Egenbetalingsloftet er i dag på 4.575 kr. per tilskudsår.
Spørgsmål nr. 3: Er forslaget konkurrenceforvridende?
”Kan ministeren garantere for, at lovforslaget er i overensstemmelse med konkurrencelovgivningen, selv om producenter af lægemidler med forslaget pålægges nye udgifter til pligtlagre, mens parallelimportørerne undtages?”
Parallelimportører og -distributører er undtaget fra lagerpligten for at undgå risikoen for, at parallelimportører trækker produkter fra det danske marked, hvilket kan forringe forsyningssituationen og kan medføre højere medicinpriser. Det skyldes, at parallelimportører og -distributører kan have vanskeligt ved at opretholde et lager, fordi de ikke kan styre deres forsyning ligesom producenter kan. Parallelimportørerne og -distributørerne vil dog fortsat være omfattet af indberetningspligten, da det er væsentligt for Lægemiddelstyrelsen at have overblik over alle virksomheders lagerbeholdninger for at overvåge og håndtere forsyningsvanskeligheder. I den sammenhæng har Konkurrence- og Forbrugerstyrelsen bemærket, at det set ud fra et konkurrencemæssigt synspunkt generelt er fornuftigt, at virksomheder stilles lige i forhold til lovpligtige krav. Det er dog i forhold til det konkrete lovforslag om lagerpligt for kritiske lægemidler Konkurrence- og Forbrugerstyrelsens umiddelbare vurdering, at den reviderede udformning af lovforslaget, hvor parallelimportører/- distributører er undtaget fra lagerpligten, er mere hensigtsmæssig for konkurrencen og markederne, end hvis parallelimportører/-distributører er omfattet af lagerkravet. Det skyldes, at forretningsmodellen og vilkårene for virksomheder, der bringer lægemidler på markedet, i forvejen er meget forskellige, og at virksomhederne tilsvarende ville have meget forskellige forudsætninger for at kunne opfylde lagerpligten. En lagerpligt, der indføres ens for alle (typer af) virksomheder, vil derfor netop ikke ramme alle virksomheder lige. En producent har, i modsætning til parallelimportører/-distributører, mere kontrol over produktionen og dermed bedre mulighed for at planlægge længere frem i tiden. Parallelimportører/-distributører har omvendt ingen indflydelse på produktionen og har ofte kun adgang til at købe mindre partier, som er i overskud hos grossisterne i andre EU-lande. Bl.a. pga. disse eksisterende forskelle i kontrol over produktionen ville lagerpligten kunne ramme parallelimportører hårdere end producenter og skabe unødige hindringer for parallelimportørernes virke på markedet, hvilket ville kunne føre til negative virkninger for konkurrencen. Med den reviderede udformning af lovforslaget minimeres denne risiko set i forhold til den oprindelige udformning af lovforslaget, og det vurderes ikke at være i strid med konkurrencereglerne. Jeg henholder mig til Konkurrence- og Forbrugerstyrelsens vurdering.
Spørgsmål 9: Krav om 14-dages levering
”Vil ministeren stille krav til parallelimportører om at kunne levere den mængde, der forventes solgt i den 14-dagsperiode, som importørerne byder ind med priser på?”
Indenrigs- og Sundhedsministeriet finder det ikke umiddelbart hensigtsmæssigt, at der fastsættes andre regler om leveringsevne ved indmeldelse af priser i en prisperiode for parallelimportørerne, end der gælder for øvrige virksomheder. Det skønnes ikke, at krav om 14-dages leveringsevne ved indmeldelse af priser i en prisperiode vil bidrage væsentligt til at løse forsyningsvanskeligheder, da de fleste forsyningsvanskeligheder strækker sig ud over 14 dage. Desuden kan et krav til parallelimportørerne om at have en leveringsevne til 14-dage betyde, at det danske marked generelt ikke får gavn af små partier af lægemidler til billige priser i samme omfang som i dag. Det nuværende generelle krav til alle virksomheder om leveringsevne til 7 dage er med til at skærpe konkurrencen på det danske marked og dermed holde priserne lavere. På den baggrund har Danmark nogle af de laveste priser i Europa på parallelimporterede og generiske lægemidler.

