Analyse
Færre lægemidler til sjældne sygdomme vurderes i Danmark
*Analyse stammer fra kampagnen Tid er liv, der blev gennemført i november og december 2024.
Kort om analysen
Danmark vurderer færre lægemidler til sjældne sygdomme end nabolande.
I Danmark er vi dårligere til at få vurderet nye lægemidler til sjældne sygdomme sammenlignet med Norge, Sverige og England.
I perioden januar 2020 til oktober 2024 godkendte Det Europæiske Lægemiddelagentur (EMA) 63 lægemidler til sjældne sygdomme.
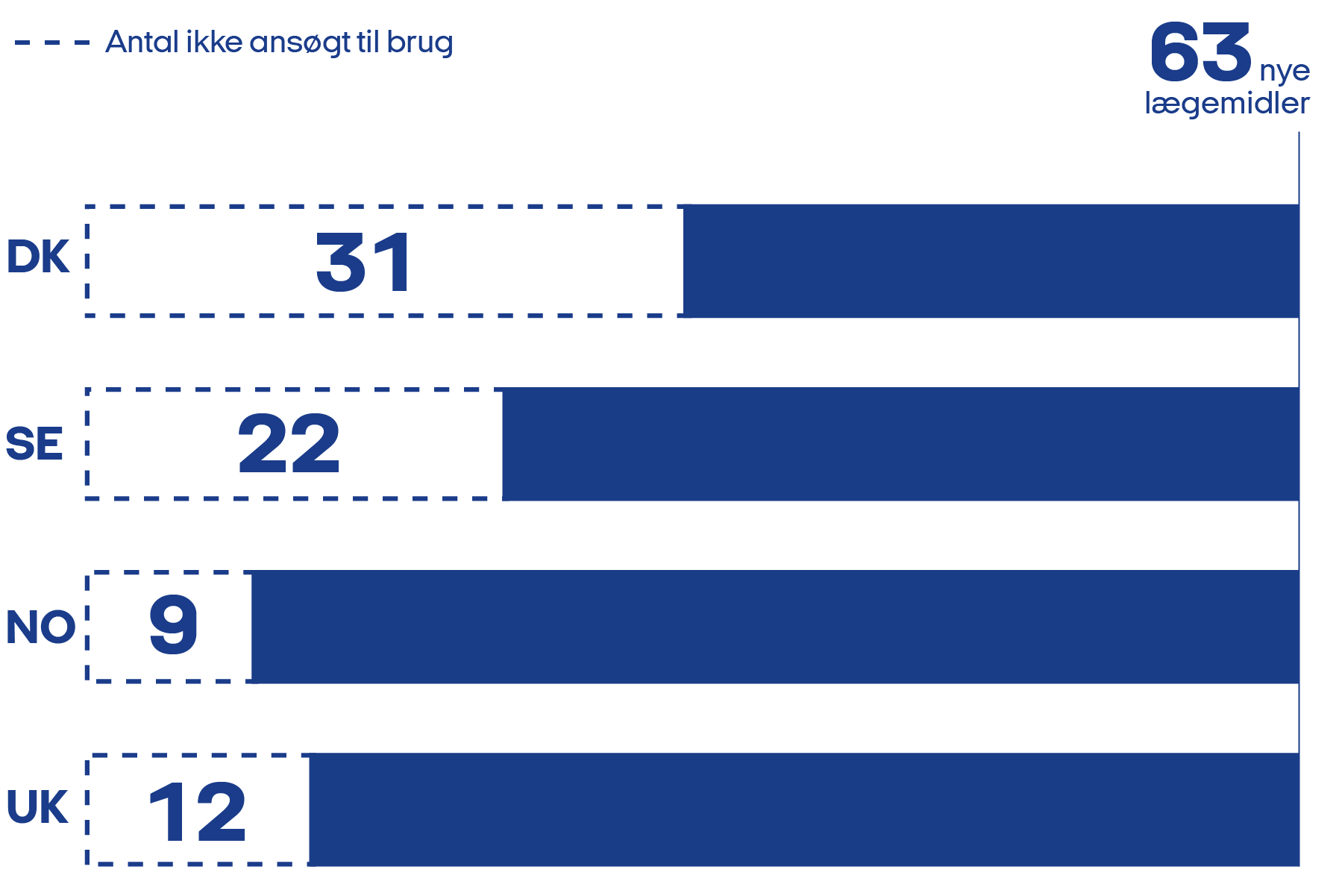
En sammenligning af de 63 lægemidler til sjældne sygdomme viser, at der i Danmark er der ikke søgt om anbefaling for hele 31 lægemidler til sjældne sygdomme, hvilket betyder, at de ikke er blevet vurderet af Medicinrådet.
I Sverige er det 22 lægemidler, 9 i Norge og 12 i England. Det betyder, at danske patienter muligvis ikke får adgang til disse nye behandlinger.
På tværs af de fire lande er det især inden for kræft, sjældne arvelige sygdomme, blodsygdomme samt lunge- og luftvejssygdomme, der er lægemidler, som ikke bliver vurderet med henblik på at blive anbefalet som standardbehandling.
Lif mener
Kompliceret proces sætter en stopper for ansøgninger
Udfordringerne ved at tage godkendte lægemidler til patienter med sjældne sygdomme i brug er endnu ikke løst. Når så relativt mange lægemidler til sjældne sygdomme ikke vurderes i Danmark, og dermed heller når ud til patienterne, kan det tyde på mere grundlæggende udfordringer. Herunder, at virksomheder ikke søger Medicinrådet om en anbefaling. Det kan skyldes flere ting.
Først og fremmest er Medicinrådets proces ressourcetung og kompliceret. Processen er den samme, uanset om behandlingen er til to danske patienter eller tusind.
For det andet er oplevelsen hos virksomhederne, at Medicinrådet har en restriktiv tilgang til vurdering af usikkerhed i data. Derfor er der også en tendens til, at lægemidler til sjældne sygdomme ofte bliver afvist på grund af sparsom evidens og dermed usikkerhed i data. For lægemidler til sjældne sygdomme, er det ofte hverken praktisk eller etisk muligt at etablere samme datagrundlag, som for mere almindelige sygdomme.
Der er bred anerkendelse af, at lægemidler til sjældne sygdomme udgør en særlig problemstilling på grund af begrænset evidens og at der dermed er større usikkerhed om størrelsen af effekt, men det bør ikke betyde, at danske patienter går glip af nye behandlinger.
Det er vigtigt, at Danmark ikke mister innovationsmuligheder. Derfor er det bekymrende, når mange af de nye behandlinger til sjældne sygdomme ikke vurderes i Danmark.
Camilla Lund-Cramer, chefkonsulent i lif
Vi er nødt til at tale om, hvorvidt vi har det rette ambitionsniveau for patienters adgang til behandling af sjældne sygdomme.
Hvad er løsningen?
1
Transparens om behandlingsmuligheder
Hvorfor kan en patient i Østdanmark ikke få en behandling, som en patient i Vestdanmark kan få? Og hvorfor kan du få en ny behandling i udlandet, som danske læger ikke kan tilbyde i Danmark? Alle patienter skal have indblik i årsager til, at de ikke kan få den behandling, som er mulige til deres sygdom.
Der skal være åbenhed om de sundhedsfaglige beslutninger for den enkelte patient.
2
Bedre adgang til individuel behandling
Værdien for den enkelte bør altid stå i centrum, når der tages beslutninger om nye lægemidler. Hver patient bør få tilbudt den bedste behandling baseret på en lægefaglig vurdering – også selvom lægemidlet er afvist som standardbehandling.
Der skal sikres lige adgang til en individuel vurdering for patienter i hele landet. Det er der ikke i dag. Selvom det er vedtaget af Folketinget.
3
Branchen tager ansvar
Usikkerhed er et uundgåeligt vilkår, når der tages nye behandlinger i brug i sundhedsvæsenet – ikke mindst når det drejer sig om lægemidler til sjældne sygdomme.
Men usikkerhed bør ikke automatisk føre til et nej til standardbehandling. Som branche er vi klar til at finde fleksible løsninger, så nye behandlinger kan komme så mange patienter som muligt til gavn. Også dem med sjældne sygdomme.
Flere analyser
Kontakt os, hvis du vil vide mere